A insuficiencia cardíaca con fracción de eyección reducida (HFrEF) é un tipo importante de insuficiencia cardíaca, e o estudo de insuficiencia cardíaca de China mostrou que o 42% das insuficiencias cardíacas en China son HFrEF, aínda que existen varias clases terapéuticas estándar de fármacos dispoñibles para a HFrEF e reduciron o risco. de morte e hospitalización por insuficiencia cardíaca en certa medida. Non obstante, os pacientes teñen un alto risco de empeoramento da insuficiencia cardíaca recorrente, a mortalidade mantense ao redor do 25% e o prognóstico segue sendo malo. Polo tanto, aínda existe unha necesidade urxente de novos axentes terapéuticos no tratamento da ICFr, e no estudo VICTORIA estudouse Vericiguat, un novo estimulador de guanilato ciclase soluble (sGC), para avaliar se Vericiguat podería mellorar o prognóstico dos pacientes con HFrEF. O estudo é un estudo de resultados clínicos de fase III, multicéntrico, aleatorizado, de grupos paralelos, controlado con placebo, dobre cego, impulsado por eventos. Realizado baixo os auspicios do Centro VIGOR de Canadá en colaboración co Instituto de Investigación Clínica Duke, participaron no estudo 616 centros de 42 países e rexións, entre eles Europa, Xapón, China e Estados Unidos. O noso departamento de cardioloxía tivo a honra de participar. Un total de 5.050 pacientes con insuficiencia cardíaca crónica de idade ≥18 anos, clase II-IV da NYHA, EF <45%, con niveis elevados de péptido natriurético (NT-proBNP) nos 30 días anteriores á aleatorización e que foran hospitalizados por insuficiencia cardíaca. dentro dos 6 meses anteriores á aleatorización ou que se administraron diuréticos por vía intravenosa para a insuficiencia cardíaca dentro dos 3 meses anteriores á aleatorización. o estudo, todos recibiron ESC, AHA/ACC e as directrices específicas nacionais/rexionales recomendadas polo estándar de atención. Os pacientes foron aleatorizados nunha proporción de 1:1 a dous grupos e foron administradosVericiguat(n=2526) e placebo (n=2524) ademais da terapia estándar, respectivamente.
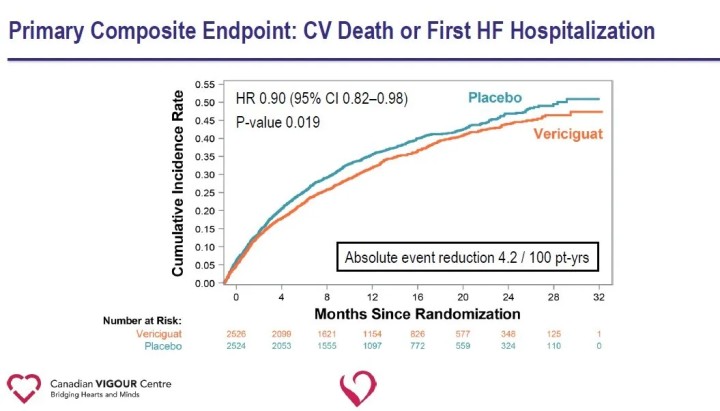
O criterio final principal do estudo foi o criterio final composto de morte cardiovascular ou primeira hospitalización por insuficiencia cardíaca; os criterios de valoración secundarios incluíron compoñentes do criterio principal, as primeiras hospitalizacións por insuficiencia cardíaca e as seguintes (primeiros eventos e recorrentes), o criterio final composto de morte por todas as causas ou hospitalización por insuficiencia cardíaca e morte por todas as causas. Cun seguimento medio de 10,8 meses, houbo unha redución relativa do 10% no criterio final primario de morte cardiovascular ou primeira hospitalización por insuficiencia cardíaca no grupo Vericiguat en comparación co grupo placebo.
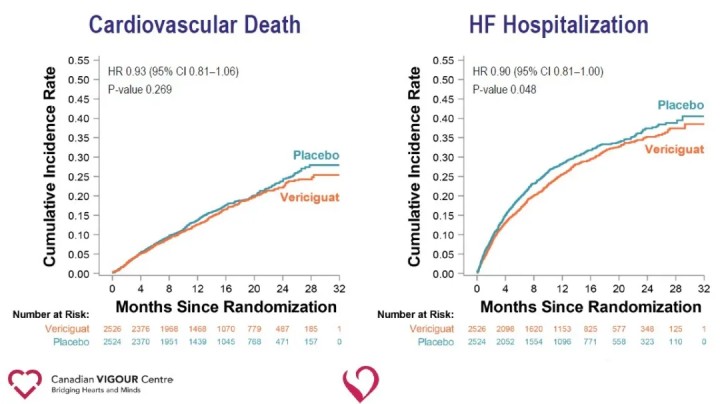
A análise dos criterios de valoración secundarios mostrou unha redución significativa da hospitalización por insuficiencia cardíaca (HR 0,90) e unha redución significativa do criterio final composto de morte por todas as causas ou hospitalización por insuficiencia cardíaca (HR 0,90) no grupo Vericiguat en comparación co grupo placebo.
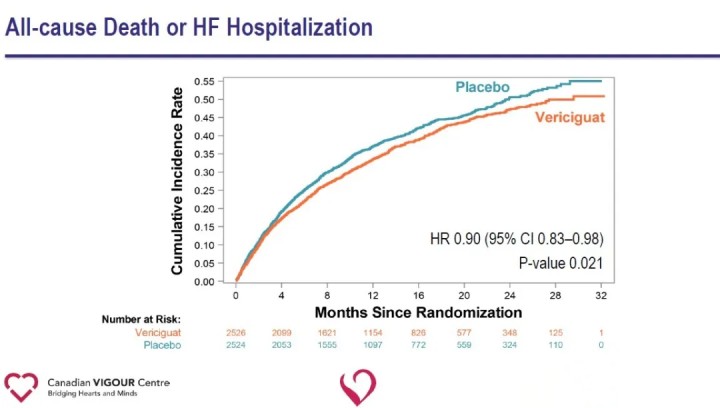
Os resultados do estudo suxiren que a adición deVericiguatao tratamento estándar da insuficiencia cardíaca reduce significativamente a aparición recente de eventos de insuficiencia cardíaca que empeoran e reduce o risco de que o punto final composto de morte cardiovascular ou hospitalización por insuficiencia cardíaca en pacientes con ICFEr. A capacidade de Vericiguat para reducir o risco do punto final composto de morte cardiovascular ou hospitalización por insuficiencia cardíaca en pacientes con insuficiencia cardíaca de alto risco proporciona unha nova vía terapéutica para a insuficiencia cardíaca e abre novas vías para a futura exploración da enfermidade cardiovascular. Vericiguat non está actualmente aprobado para comercialización. A seguridade, a eficacia e a rendibilidade do medicamento aínda deben ser probadas máis no mercado.
Hora de publicación: 09-02-2022
